考点38 碳的单质
⒈金刚石、石墨的物理性质和用途的比较
金刚石(由碳元素组成) | 石墨(由碳元素组成) | |
硬度 | 最硬 | 软,在纸上可留下痕迹 |
熔点 | 很高 | 高、耐高温 |
导电性 | 不导电 | 导电(良好) |
导热性 | 无 | 良好 |
用途 | 钻探机钻头、刻刀 | 铅笔芯、润滑剂、电极等 |
结论 | 碳单质的物理性质不同,是由于金刚石、石墨中碳原子的排列不同 |
得到启示:⑴结构决定性质,性质决定用途;⑵同一种元素可以组成不同的单质。
⒉木炭、活性炭
⑴木炭:有吸附作用,用于吸附一些食品和工业产品里的色素,吸附有异味的物质。
⑵活性炭:有较强的吸附作用,用于防毒面具、冰箱的除臭剂。
考点39 碳的化学性质
⒈常温下,碳的化学性质不活泼(碳原子最外层有4 个电子)
应用:解释古代字画经历几千年而不变色、档案资料要求用碳素墨水书写
⒉碳的可燃性(相同的反应物,因反应物的量不同,生成物可能不同)
充分燃烧C + O2===== CO2——放热
放热
不充分燃烧2C + O2===== 2CO——放热
⒊碳的还原性(以木炭还原CuO为例)——用于冶炼金属
⑴现象:黑色粉末变红色,澄清的石灰水变浑浊。
⑵化学方程式:C + 2CuO ===== 2Cu + CO2↑
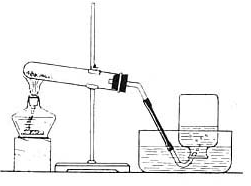
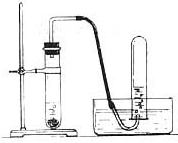
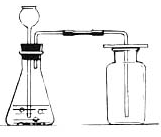
考点40 实验室制取气体的装置选择
⒈发生装置的选择依据
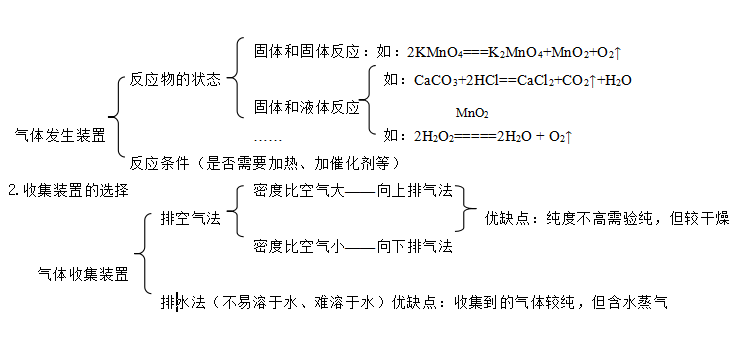
氧气(O2) | 氢气(H2) | 二氧化碳(CO2) | |
反应原理 | 2KClO32KCl + 3O2↑ 2KMnO4K2MnO4+MnO2+O2↑ | Zn +H2SO4==ZnSO4+H2↑ Zn + 2HCl =ZnCl2+ H2↑ | CaCO3+2HCl==CaCl2+H2O+CO2↑ |
发生装置 |
|
|
|
收集方法 | ①向上排空气法(密度比空气大); ②排水法(不易溶于水) | ①向下排空气法(密度比空气小); ②排水法(难溶于水) | 只能用向上排空气法(密度比空气大,能溶于水) |
操作步骤 | ①组装仪器②检查装置的气密性③装药品④固定装置⑤加热⑥收集气体⑦把导管撤出水槽⑧熄灭酒精灯。 | ①组装仪器②检查装置的气密性③加药品④验纯⑤收集气体 | ①组装仪器②检查装置的气密性③加入大理石④从漏斗注入稀盐酸⑤收集气体 |
验 满 | 向上排空气法收集时,用带火星的木条放在集气瓶口,木条复燃,说明收集已满。排水法收集时,气泡往集气瓶外冒时,收集已满。 | 用排水法收集时,当气泡往外冒时,说明收集已满。 | 用燃着的木条放在集气瓶口,若木条熄灭,说明收集已满。 |
检验或验纯 | 验证:用带火星木条伸入集气瓶内,木条复燃,说明是氧气 | 验纯:用排水法收集一试管氢气,用大拇指堵住,管口向下,移近酒精灯火焰,若发出微弱的“噗”的一声,说明氢气已纯,若发出尖锐的爆鸣声,说明氢气不纯。 | 验证:通入澄清石灰水,石灰水变浑浊,说明是二氧化碳。 [CO2+Ca(OH)2==CaCO3↓+H2O] |
注 意 事 项 | 排水法收集时当气泡连续均匀冒出时开始收集,以免收集气体不纯;排水法收集完后,先将导管移出水槽,再停止加热,以免水槽中的水倒流至热试管,使试管炸裂。 | 长颈漏斗下端应伸入液面以下,以免生成的气体从长颈漏斗中逸出;用排空气法收集时,导管应伸入集气瓶底部; | 不能用稀H2SO4代替稀盐酸,因为稀H2SO4与石灰石反应生成微溶性的CaSO4覆盖在CaCO3表面,从而阻止反应的进一步进行。 |
考点41 实验室制取二氧化碳
⒈药品:大理石(或石灰石)、稀盐酸(不要写成CaCO3和稀盐酸)
⒉原理:CaCO3+ 2HCl == CaCl2+ H2O + CO2↑
注意:⑴不能用浓盐酸代替稀盐酸,因为浓盐酸易挥发,使制得的CO2不纯(混有氯化氢气体);⑵不能用稀硫酸代替稀盐酸,因为稀硫酸与CaCO3反应生成微溶于水的硫酸钙覆盖在大理石(或石灰石)的表面,阻止反应的进行;⑶不能用Na2CO3代替大理石(或石灰石),因为Na2CO3与稀盐酸的反应速度太快,不便于收集。
⒊发生装置:固 + 液——气体型(参看课本P111图6-10)
⒋收集装置:只用向上排空气法(因为CO2能溶于水,密度比空气大)
⒌CO2的检验:将气体通入澄清的石灰水中,如果石灰水变浑浊,则该气体为CO2。
化学方程式:CO2+ Ca(OH)2== CaCO3↓+ H2O
⒍CO2的验满:用燃着的木条放在集气瓶口,如果木条熄灭,则已充满。(这样做是利用CO2不能燃烧、不支持燃烧的性质)。
⒎CO2的工业制法:CaCO3====CaO + CO2↑
⒏实验室制取CO2的实验操作过程
⑴检查装置的气密性;⑵装入大理石,塞紧胶塞;⑶固定装置;⑷从长颈漏斗加入稀盐酸至长颈漏斗下端管口液封;⑸收集气体,导管一定要伸入集气瓶底部;⑹检验是否集满。
考点42 实验室制取气体的一般设计思路和方法
⒈药品的选择原则:选择反应速度适中,价格便宜,来源广泛,污染少,实验安全,所制气体纯净的药品。
⒉实验装置的设计:根据药品的状态和反应原理,以及反应条件设计装置。装置设计要简单,便于控制和操作。
考点43 二氧化碳的性质
⒈二氧化碳的物理性质:⑴常温下是无色无味的气体(CO2固体叫“干冰”);
⑵密度比空气大;
⑶能溶于水;(设计实验证明,参看课本P114实验6-5)
⒉二氧化碳的化学性质
⑴二氧化碳不能燃烧,也不能支持燃烧(实验探究:参看课本P113实验6-4),二氧化碳不供给呼吸(解释“屠狗洞”现象、灯火实验)
⑵二氧化碳能与水反应生成碳酸(实验探究:参看课本P114实验6-6)
化学方程式:CO2+ H2O == H2CO3碳酸不稳定,H2CO3== CO2↑+ H2O
⑶二氧化碳与石灰水、烧碱反应
现象:澄清的石灰水变浑浊。原因:生成不溶于水的白色CaCO3沉淀。
化学方程式:CO2+ Ca(OH)2== CaCO3↓+ H2O

⑷二氧化碳能与炽热的碳反应
CO2+ C ====2CO
考点44 二氧化碳对生活和环境的影响
⒈二氧化碳的用途:⑴灭火;⑵作致冷剂如人工降雨、舞台烟雾;⑶制碳酸饮料;⑷作温室肥料等
⒉温室效应:由于二氧化碳的过多排放
温室效应的危害:全球变暖,两极冰川融化,海平面升高,淹没沿海地带土地沙漠化,旱涝灾害,
农业减产
⒊控制温室效应的措施
措施:减少煤、石油、天然气等化石燃料的使用,开发利用太阳能、风能、乙醇等清洁能源
大力植树造林,严禁乱砍滥伐
考点45 一氧化碳的性质
⒈物理性质:通常情况下是无色无味的气体,难溶于水,密度比空气略小。(实验室制取CO只能用排水法收集)。想一想:水能防止CO中毒吗?
⒉化学性质
⑴可燃性: 2CO + O2====2CO2——作燃料(是煤气的主要成分)
现象: 产生蓝色火焰,放出热量,产生能使澄清石灰水变浑浊的气体。
⑵还原性:
CO + CuO====Cu + CO2——冶炼金属
现象:黑色粉末变红色,澄清的石灰水变浑浊
注意:①操作顺序实验时,先通CO,后加热;实验完毕,先停止加热,继续通CO直至玻璃管冷却;
②但需对尾气处理,方法是将CO点燃转变CO2(或收集起来)。
⑶毒性:CO能与血液中的血红蛋白结合,使血红蛋白失去运输氧气的能力,使人因缺氧而死亡。
<p style="border: 0px; margin-top: 0.63em; margin-bottom: 1.8em; padding: 0px; counter-reset: list-1 0 list-2 0 list-3 0 list-4 0 l