一、配制一定物质的量浓度的溶液
以配制100mL1.00mol/L的NaOH溶液为例:
1、步骤:
(1)计算 (2)称量:4.0g(保留一位小数)(3)溶解(4)转移:待烧杯中溶液冷却至室温后转移(5)洗涤 (6)定容:将蒸馏水注入容量瓶,当液面离刻度线1—2cm时,改用胶头滴管滴加蒸馏水至凹液面最低点与刻度线在同一水平线上(7)摇匀:盖好瓶塞,上下颠倒、摇匀 (8)装瓶贴标签 :标签上注明药品的名称、浓度。
2、所用仪器:(由步骤写仪器)
托盘天平、药匙、烧杯、玻璃棒、(量筒)、100mL容量瓶、胶头滴管
3、注意事项:
(1) 容量瓶:只有一个刻度线且标有使用温度和量程规格,只能配制瓶上规定容积的溶液。(另外使用温度和量程规格还有滴定管、量筒
(2) 常见的容量瓶:50 mL、100mL、250mL、500mL、1000mL。若配制480mL与240mL溶液,应分别用500mL容量瓶和250mL容量瓶。写所用仪器时,容量瓶必须注明规格,托盘天平不能写成托盘天秤!
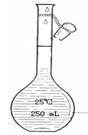
(3) 容量瓶使用之前必须查漏。
方法:向容量瓶内加少量水,塞好瓶塞,用食指顶住瓶塞,用另一只手的五指托住瓶底,把瓶倒立过来,如不漏水,正立,把瓶塞旋转1800后塞紧,再倒立若不漏水,方可使用。(分液漏斗与滴定管使用前也要查漏)
(4)命题角度:一计算所需的固体和液体的量,二是仪器的缺失与选择,三是实验误差分析。
二、Fe(OH)3胶体的制备:
1、步骤:
向沸水中加入FeCl3的饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
操作要点:四步曲:①先煮沸,②加入饱和的FeCl3溶液,③再煮沸至红褐色,④停止加热
2、涉及的化学方程式:
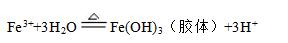
强调之一是用等号,强调之二是标明胶体而不是沉淀,强调之三是加热。
3、命题角度:
配制步骤及对应离子方程式的书写
三、焰色反应:
1、 步骤:洗—烧—蘸—烧—洗—烧
2 、该实验用铂丝或铁丝
3 、焰色反应可以是单质,也可以是化合物,是物理性质
4 、Na ,K 的焰色:黄色,紫色(透过蓝色的钴玻璃)
5 、某物质作焰色反应,有黄色火焰一定有Na ,可能有K
6、命题角度:实验操作步骤及Na ,K 的焰色
四、Fe(OH)2的制备:
1、实验现象:
白色沉淀立即转化灰绿色,最后变成红褐色沉淀。
2、化学方程式为:
Fe2++2OH-=Fe(OH)2 4e(OH)2+O2+2H2O= 4e(OH)3
3、注意事项:
(1)所用亚铁盐溶液必须是新制的,NaOH溶液必须煮沸,(2)滴定管须插入液以下,
(3)往往在液面加一层油膜,如苯或食物油等(以防止氧气的氧化)。
4、命题角度:
制备过程中的现象、方程式书写及有关采取措施的原因
五、硅酸的制备:
1、步骤:
在试管中加入3—5mL饱和Na2SiO3溶液,滴入1—2滴酚酞溶液,再用胶头滴管逐滴加入稀盐酸,边加边振荡,至溶液颜色变浅并接近消失时停止。
2、现象:
有透明的硅酸凝胶形成
3、化学方程式:
NaSiO3+2HCl= H2SiO3↓+2NaCl(强酸制弱酸)
4、NaSiO3溶液由于SiO32-水解而显碱性,从而使酚酞试液呈红色。
六、重要离子的检验:
1、Cl-的检验:
加入AgNO3溶液,再加入稀硝酸,若生成不溶于稀HNO3的白色沉淀;或先加硝酸化溶液(排除CO32-干扰),再滴加AgNO3溶液,如有白色沉淀生成,则说明有Cl-存在
2、SO42-的检验:
先加入盐酸,若有白色沉淀,先进行过滤,在滤液中再加入BaCl2溶液,生成白色沉淀即可证明。若无沉淀,则在溶液中直接滴入BaCl2溶液进行检验。
命题角度:
检验方法、除杂、沉淀洗涤及相关纯度的计算
七、氨气的实验室制法
1、反应原理 :
2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
2、收集:
向下排空气法(管口塞一团棉花,避免空气对流)
3、验满:
①将湿润的红色石蕊试纸放在试管口,若试纸变蓝,说明氨气已收集满 ②将蘸有浓盐酸的玻璃棒靠近试管口,出现大量白烟,则证明氨气已收集满
4、干燥方法:
碱石灰干燥(不能无水氯化钙)
5、装置图:
固体和固体加热制气体的装置,与制氧气的相同
拓展:
浓氨水或浓铵溶液滴到生石灰或烧碱中制氨气,或浓氨水直接加热也可制氨气
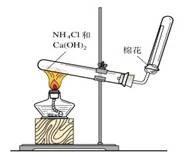
6、命题角度:
因氨气作为中学化学实验制取气体中唯一的实验,其地位不可估量。
主要角度为:
反应原理、收集、干燥及验满等,并以此基础进行性质探究实验。
八、喷泉实验
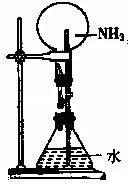
1、实验原理:
氨气极易溶于水,挤压胶头滴管,少量的水即可溶解大量的氨气(1:700),使烧瓶内压强迅速减小,外界大气压将烧杯中的水压入上面的烧瓶,故NH3、HCl、HBr 、HI、 SO2 等气体均能溶于水形成喷泉。
2、实验现象:
产生红色喷泉(氨气溶于水形成碱性溶液,酚酞遇碱显红色)
3、实验关键:
①氨气应充满 ②烧瓶应干燥 ③装置不得漏气
4、实验拓展:
CO2、H2S、Cl2等与水不能形成喷泉,但与NaOH溶液可形成喷泉
九、铜与浓硫酸反应的实验
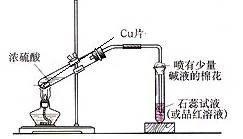
1、实验原理:
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
2、现象:
加热之后,试管中的品红溶液褪色,或试管中的紫色石蕊试液变红;将反应后的溶液倒入盛有水的烧杯中,溶液由黑色变成蓝色。
3、原因解释:
变黑的物质为被浓硫酸氧化生成CuO,CuO与冲稀的硫酸反应生成了CuSO4溶液。
【提示】
由于此反应快,利用铜丝,便于及时抽出,减少污染。
命题角度:
SO2的性质及产物的探究、“绿色化学”及尾气的处理等。
十、铝热反应:
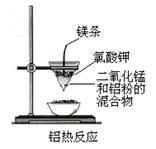
1、实验操作步骤:
把少量干燥的氧化铁和适量的铝粉均匀混合后放在纸漏斗中,在混合物上面加少量氯酸钾固体中,中间插一根用砂纸打磨过的镁条,点燃。
2、实验现象:
立即剧烈反应,发出耀眼的光芒,产生大量的烟,纸漏斗被烧破,有红热状态的液珠,落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
3、化学反应方程式:
Fe2O3+2Al2Fe+Al2O3
4、注意事项:
(1)要用打磨净的镁条表面的氧化膜,否则难以点燃。
(2)玻璃漏斗内的纸漏斗要厚一些,并用水润湿,以防损坏漏斗
(3)蒸发皿要垫适量的细沙:一是防止蒸发皿炸裂,二是防止熔融的液体溅出伤人。
(4)实验装置不要距人太近,防止使人受伤。
5、命题角度:
实验操作步骤及化学方程式。
十一、中和热实验(了解):
1、概念:
酸与碱发生中和反应生成1 mol水时所释放的热量
注意:
(1)酸、碱分别是强酸、强碱 对应的方程式:H++OH-=H2O △H=-57.3KJ/mol
(2)数值固定不变,它与燃烧热一样,因具有明确的含义,故文字表达时不带正负号。
2、中和热的测定注意事项:
(1)为了减少误差,必须确保热量尽可能的少损失,实验重复两次,去测量数据的平均值作计算依据
(2)为了保证酸碱完全中和常采用H+或OH-稍稍过量的方法
(3)实验若使用了弱酸或弱碱,引种和过程中电离吸热,会使测得的中和热数值偏小
十二、酸碱中和滴定实验(了解):
(以一元酸与一元碱中和滴定为例)
1、原理:C酸V酸=C碱V碱
2、要求:①准确测算的体积. ②准确判断滴定终点
3、酸式滴定管和碱式滴定管的构造:



